Ideální plyn a děje v plynech
Rychlost
Rychlost, kterou se pohybují molekuly v plynu není stejná u všech molekul. Proto se musí najít taková rychlost, jakou by měly molekuly plynu o dané vnitřní energii, kdyby měly všechny stejnou rychlost.
Rychlost, kterou by všechny molekuly měly, kdyby měly všechny tuto rychlost a stejnou kinetickou energii jako ve skutečnosti, je kvadratická rychlost vk.
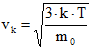
k je Boltzmannova konstanta k = 1,38 × 10–23 J × K–1
m0….hmotnost molekuly
Vnitřní energie plynu je celková kinetická energie všech molekul plynu
Střední kinetická energie, kterou mají molekuly plynu, je přímo úměrná termodynamické teplotě plynu.
střední kinetická energie:
![]()
Druhá mocnina střední kvadratické rychlosti je aritmetický průměr druhých mocnin rychlostí všech molekul
Tlak
– Souvisí s otázkou 28
Tlak plynu není stálý, ale stále se pohybuje kolem určité střední hodnoty – tento stav se nazývá fluktuace tlaku. Střední hodnota tlaku je
![]()
Když dosadím vk z předchozí vzorce, vyjde mi stavová rovnice plynu (popisuje termodynamický stav ideálního plynu):
p × V = N × k × T
Když vyjádříme počet molekul N = n × NA, můžeme nahradit součin Boltzmannovy konstanty k a Avogadrovy konstanty Na jednou konstantou → molární (univerzální) plynová konstanta Rm(někdy jen R) = NA × k = 8,314 J × K–1 × mol–1(tabulky 153)
p × V = n × Rm × T
Látkové množství lze určit podílem hmotnosti plynu m v gramech a molární hmotnosti plynu Mm (stejná hodnota jako molekulová relativní hmotnost Mr) – více otázka 28 – látkové množství.
n = m / Mm
p * v = m / Mm * Rm * T
Tepelné děje v plynech
Při tepelných dějích se mění hodnoty stavových veličin. Průběh tepelných dějů se zakresluje do pV diagramu. Teplotu lze určit z hodnot tlaku a objemu.
Izotermický děj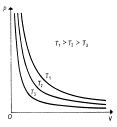
Teplota se nemění → T = konst.
Ze stavové rovnice vyplyne →
p × V = konst.
p1 × V1 = p2 × V2
Nemění se teplota -> nemění se vnitřní energie
ΔU = 0 => Q = – W = W¢
Teplo přijaté ideálním plynem při izotermickém ději se rovná práci, kterou plyn při tomto ději vykoná. Grafem je izoterma
Izochorický děj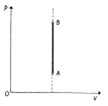
Objem se nemění → V = konst.
Ze stavové rovnice vyplyne →
![]()
![]() Nemění se objem plynu -> práce plynu je nulová -> mění se vnitř. energie
Nemění se objem plynu -> práce plynu je nulová -> mění se vnitř. energie
ΔU = QV
QV = m × cV × ΔT, cV je měrná tepelná kapacita plynu při stálém objemu
Teplo přijaté ideálním plynem při izochorickém ději se rovnu přírůstku jeho vnitřní energie. Grafem je izochora
Izobarický děj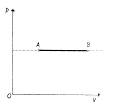
Tlak plynu se nemění → p = konst.
Ze stavové rovnice vyplyne → ![]()
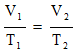
Zvýšíme-li teplotu ideálního plynu stálé hmotnosti izobaricky o stejnou hodnotu ΔT jako u děje izochorického, přijme plyn teplo
Qp = m × cp × ΔT, cp je měrná tepelná kapacita plynu při stálém tlaku
Grafem je izobara
Protože se teplota při izobarickém ději zvýšila o stejnou teplotu jako u izochorického děje, je změna vnitřní energie u obou dějů stejná. Teplo přijaté při izobarickém ději je ale větší, protože se musí ještě vykonat práce při rozpínání plynu. Proto je i cp > cV.
Adiabatický děj
Při adiabatickém ději je teplo, které si předala soustava s okolím, nulové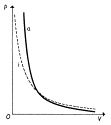
Q = 0 ΔU = W
– Přerušovaná v grafu je izoterma (méně strmá)
→ adiabaticky izolovaná soustava je taková soustava, u které nemůže dojít k tepelné výměně mezi ní a okolním prostředím, ale může dojít k silovému působení a tím ke konání práce.
Pro adiabatický děj platí Poissonův zákon:
![]()
pro určení teploty platí stavová rovnice a vztah z ní odvozený →
![]()
κ je Poissonova konstanta
![]() ; – měrná tepelná kapacita při stálém P a V
; – měrná tepelná kapacita při stálém P a V
κ > 1. Pro plyn s jednoatomovými molekulami κ ≈ 5/3, pro plyn s dvouatomovými molekulami κ ≈ 7/5
Pomocí pV diagramu lze snadno určit práci, kterou ideální plyn vykoná.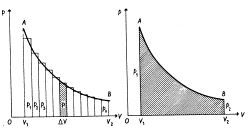
W = = p ×ΔV
Kruhový děj
Pokud termodynamická soustava projde řadou změn a nakonec se vrátí do původního stavu, pak říkáme, že soustava vykonala kruhový děj.
= děj, při němž je konečný stav soustavy totožný s počátečním stavem. Obsah plochy uvnitř křivky ( v diagramu p-V) znázorňuje celkovou práci W´ vykonanou během jednoho cyklu
Na principu kruhového děje pracují tepelné stroje – motory, parní stroj (ohřívají se a chladí).
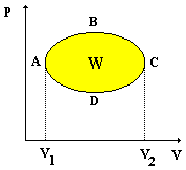 Práce vykonaná plynem při kruhovém ději vyznačuje horní křivka (AC), práci, kterou jsme plynu museli dodat, aby se vrátil do původního stavu vyznačuje spodní křivka (CA).
Práce vykonaná plynem při kruhovém ději vyznačuje horní křivka (AC), práci, kterou jsme plynu museli dodat, aby se vrátil do původního stavu vyznačuje spodní křivka (CA).
Ideální kruhový děj by byl asi doslova kruhový, technicky je však nejužívanější Carnotův cyklus – z adiabatických a izotermických dějů.
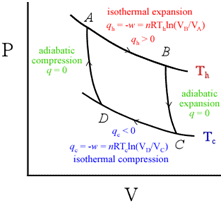 Při jednotlivých částech kruhového děje se plyn ohřívá nebo ochlazuje.
Při jednotlivých částech kruhového děje se plyn ohřívá nebo ochlazuje.
Každý tepelný stroj má dvě části – ohřívač (dodává teplo Q1, ohřívá plyn) a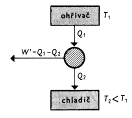 chladič (přijímá teplo Q2, ochlazuje plyn). Chladič má vždy teplotu menší než ohřívač.
chladič (přijímá teplo Q2, ochlazuje plyn). Chladič má vždy teplotu menší než ohřívač.
Pro teoretickou účinnost kruhového děje platí
![]()
Q1 je teplo plynu dodané, Q2 teplo plynu odebrané. T1 je nejvyšší teplota v cyklu, T2 je nejnižší teplota cyklu.
Reálná účinnost tepelných strojů je ještě menší.
W‘ = Q1 – Q2 (jedno vyberu a jedno odevzdám, proto mínus)
Kvůli tomu, že pracuje v malém rozsahu teplot, má parní stroj nízkou účinnost.
Druhý termodynamický zákon
Není možné sestrojit periodicky pracující tepelný stroj, který by jen přijímal teplo od určitého tělesa (ohřívače) a vykonával stejně velkou práci. Tzn. nelze sestrojit perpetuum mobile druhého druhu (termodynamické; prvního druhu je mechanické).
Není možné, aby při tepelné výměně těleso o vyšší teplotě přijímalo teplo ze studenějšího tělesa.
Tomuto neodpírá lednička, kde se konáním práce zmenšuje teplota a teplo se odvádí.
Tepelné motory
– jsou to hnací stroje, které přeměňují vnitřní energii (z paliva se uvolní hořením) na pohybovou rotační
Parní :
Parní stroj – vynálezce Thomas Savery, postupně byl několikrát zdokonalen, nejvýznamněji Jamesem Wattem, který umožnil jeho využití v průmyslu a odstartoval průmyslovou revoluci ve Spojeném království. Účinnost takového stroje je 5 – 15%.
Pára z kotle svým tlakem způsobuje posuvný pohyb pístu, který je přenášen klikou na kolo, kde vzniká pohyb otáčivý.
Parní turbína
= točivý tepelný stroj, který přeměňuje tepelnou energii proudící páry na rotační pohyb. Do dnešních dnů se využívá v tepelných elektrárnách, kde ji roztáčí pára z kotle spalující úhlí.
Spalovací motory
Zážehové spalovací motory
– Palivem je benzin
Dalším dělením bychom si je mohli rozlišit na dvoutaktní a čtyřtaktní. Dvoutaktní najdou dnes využítí v zahradních strojích, např. motorové pily. Dříve se používaly i do aut – trabant, warburg. Do takového motoru nešlo ovšem nalít jen benzín, bylo nutné spolu s benzínem přidat i olej.
Počet taktů je odvozen od počtu kroků, které se opakují.
Dvoutaktní motor – pracovní cyklus tohoto motoru proběhne za jednu otáčku. Účinnost je oproti čtyřtaktnímu motoru nižší a také ekologické hledisko není nezanedbatelné (olej v palivu). Na druhou stranu jsou ovšem lehčí, za stejný čas poskytují vyšší výkon než čtyřdobé.
Fáze činnosti:
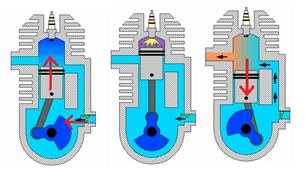 1. Sání a komprese: píst se pohybuje nahoru. U hřídele vzniká podtlak a nasává palivo. Po nasátí se uzavírá jak nasávací, tak i přepouštěcí ventil (šipky vpravo na obrázku) a palivo z minulého nasátí se stlačuje – nastává koprese. V prostoru pod pístem se znova objeví podtlak a palivo se nasaje do prostoru hřídele.
1. Sání a komprese: píst se pohybuje nahoru. U hřídele vzniká podtlak a nasává palivo. Po nasátí se uzavírá jak nasávací, tak i přepouštěcí ventil (šipky vpravo na obrázku) a palivo z minulého nasátí se stlačuje – nastává koprese. V prostoru pod pístem se znova objeví podtlak a palivo se nasaje do prostoru hřídele.
- Expanze a výfuk – těsně před vrcholem pístu přeskočí ze svíčky jiskra a dochází k zážehu (výbuchu). Nastává expanze a píst je silou tlačen dolů – píst pracuje. Otevírá se výfuk a spodní hrana pístu vytlačuje nové palivo přepouštěcím ventilem nahoru, které vytlačí spaliny výfukem ven. (vysvětlit svíčku, že výboj prorazí na krátkou chvíli el. pevnost vzduchu)
Čtyřtaktní motor – pracovní cyklus tohoto motoru proběhne za 2 otáčky. Pohonná směs neobsahuje olej, nemá 2 a 2 fáze sloučeny jako dvoutaktní, ale zvlášť. Složitější a účinnější, nemá připouštěcí kanálek, směs je pouze nad pístem.
Vznětové spalovací motory (dieselové)
– Palivem je nafta, pracuje podobně jako zážehové motory, ale palivo je dodáváno odděleně od vzduchu, vzduch je stlačen pístem, což vyvolá velkou teplotu a tam je poté vstríknuta nafta, která se samovznítí, není potřeba jiskry. Jsou větší, používají se spíše do větších strojů, menší životnost.